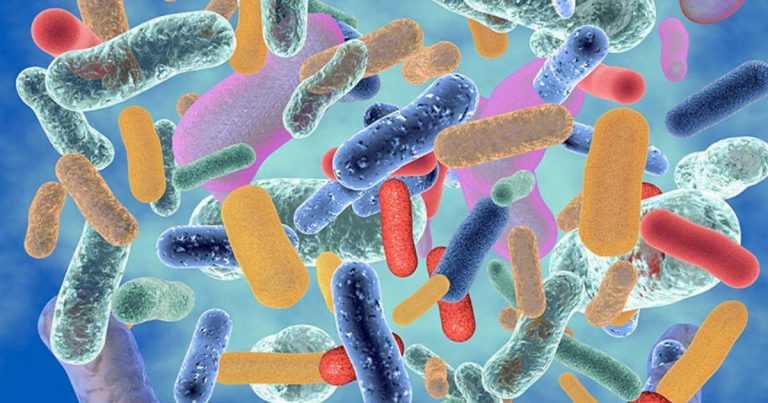
Mikrobiota je zajednički naziv za sve mikroorganizme koji žive i u telu čoveka.
Mikrobiota uključuje bakterije, arheje, protozoe gljivice i virusie. Postoji mikrobiota želudca, tankog creva, debelog creva, kao i mikrobiota kože, vagine, itd. Pri tome, najveći broj mikroorganizama koji se nalaze u telu čoveka, žive u debelom crevu.
U debelom crevu se nalazi preko 70% svih mikroba koji se nalaze u telu čoveka i crevnoj flori.
Genetska komponenta mikrobiote naziva se Mikrobiom.
Mikrobiom je integralan deo mikroorganizma i neophodan je za pravilnu funkciju organa.
Individualne vrste mikroorganizama u mikrobioti su dugo smatrane „komensalnim“ organizmima – što bukvalno znači „za istim stolom“ – sa implikacijom da takvi mikroorganizmi nisu ni patogeni, ni štetni kada su na svom fizičkom mestu i u dobrom odnosu sa drugim mikroorganizmima.
U ovom članku saznaćete:

Članak pripremila: Dr med. biohemije Milka Popović – praktičar funkcionalne medicine
Sa rođenjem, naš probavni sistem je nerazvijen i nestabilan. Nakon što dete dostigne 2 – 3 godine života, dostiže se relativna stabilnost u vidu sastava mikrobiote u debelom crevu.
Bogatstvo i raznovrsnost crevne mikrobiote oblikovane u ranim godinama života, karakteriše zdrav crevni mikrobiom.
Međutim, kompozicija optimalne, zdrave mikrobiote je drugačija za svakog pojedinca.
Sastav mikrobioma osobe je veoma promenljiv i može se promeniti u zavisnosti od starosti, etničkog porekla, geografske lokacije življenja, ishrane, životnog stila, lekova i ekoloških faktora.
Iako se ranije smatralo da se crevna mikrobiota sastoji od 500-1000 vrsta mikroba, na bazi nedavno sprovedenog velikog istraživanja, procenjeno je da je ukupna mikroflora ljudskih creva sačinjena od preko 35000 vrsta bakterija [1].
Mikrobiom zdravih odraslih osoba dominantno sačinjavaju četiri grupe bakterija:
Tradicionalno, odnos Firmicutes vs. Bacteriodetes ukazuje na predispozicije za bolesna stanja [3].
Iako je ovaj opšti profil ostaje konstantan, mikrobiota creva pokazuje vremenske i prostorne razlike u distribuciji, u rodu, nivou i šire.
Počev od jednjaka distalno do rektuma, može se identifikovati razlika u raznolikosti i broju bakterija u rasponu od 10 1 do 1012 bakterija po gramu sadržaja tj. fecesa.
Streptokok (Streptococcus) je dominantan rod u distalnom jednjaku, dvanaestopalačnom crevu.
Helicobacter je dominantni rod u želudcu i određuje mikrobni pejzaž želučane flore. Kada Helicobacter pylorinastanjuje želudac kao komensalna bakterija, postoji bogata raznolikost koju čine drugi dominantni rodovi kao što su Streptococcus, Prevotella, Veillonella i Rothia [2].
Ova raznolikost se smanjuje kada Helicobacter pylori stekne patogen karakter.
Mikrobiota creva održava simbiotski odnos sa sluznicom creva i kao takva ima značajanu metaboličku, imunološku i crevno-zaštitnu funkciju kod zdravog pojedinca.
Mikrobiota creva, koja dobija hranjive sastojke iz ishrane domaćina, je organ sama po sebi koja ima široku metaboličku sposobnost i funkcionalni značaj.
Mikrobiota creva ima sledeće funkcije:
Mikrobiota creva u velikoj meri proizvodi hranjive sastojke od ugljenih hidrata koje dobija od svog domaćina.
Fermentacija ugljenih hidrata koji se nisu svarili i nesvarljivi oligosaharidi se vrši uz pomoć bakterija kao što su Bacteroides, Roseburia, Bifidobacterium, Fecalibacterium i Enterobacteria.
Kao product proizvode se kratkolančane masne kiseline (SCFA), kao što su butirat, propionat i acetat, koji su bogati izvori energije za domaćina.
Takođe je dokazano da mikrobiota creva pozitivno utiče na metabolizam masti suzbijanjem inhibicije aktivnosti lipoprotein lipaze u adipocitima, kao i da Bacteroides podspešuju varenje lipida [4].
Isto tako, efikasno učestvuje u metabolizmu proteina koristeći svoje enzime koji razlažu proteine.
Nekoliko transportera aminokiselina na ćelijskom zidu bakterija olakšava ulazak aminokiselina iz crevnog lumena u bakterije, pri čemu bakterije dalje pretvaraju amino kiseline u male antimikrobne molekule zvane bakteriocini.
Sinteza vitamina K i nekoliko komponenti vitamina B je još jedna glavna metabolička funkcija mikrobiote creva.
Pripadnici roda Bacteroides su pokazali da sintetišu konjugovanu linoleinsku kiselinu (CLA) za koju se zna da ima antidijabetična, antiaterogenična, antigojazna, hipolipidemična i imunomodulatorna svojstva [5].
Mikrobiota creva, naročito Bacteroides intestinalis, u nekoj meri I Bacteroides fragilis i E. coli imaju sposobnost dekonjugacije i dehidracije primarne žučne kiseline i pretvaraju ih u sekundarne žučne kiseline u debelom crevu [6].
Takođe, normalna mikrobiota creva pozitivno utiče na energetski metabolizam ćelija i time doprinosi celokupnom zdravlju čoveka [7].
Sposobnost mikrobioma creva da metabolišu ksenobiotike i lekove je prvi put prepoznato pre više od 40 godina. Sada imamo mnogo više dokaza i možemo reći da poznajemo ulogu crevne mikrobiote u metabolizmu ksenobiotika.
Ksenobiotik je hemijska supstanca koja je prisutna u organizmu, ali se u njemu ne proizvodi niti se očekuje da bude prisutna. U ksenobiotike se mogu svrstati i supstance koje su u organizmu prisutne u mnogo većoj koncentraciji od uobičajene. Konkretno, lekovi kao što su antibiotici su ksenobiotici za ljude, jer ih ljudsko telo ne proizvodi, niti su deo njihove normalne ishrane.
Njihova uloga u ovom metabolizmu može da ima veliki uticaj na terapiju raznih bolesti u budućnosti. Istraživanja Claitona i drugih [8] su pokazala da pojedini substance koje proizvode crevne bakterije, mogu da smanje sposobnost jetre da metaboliše neke lekove kao npr.acetaminophen.
Kako bi gastrointestinalni trakt bio zdrav, neophodno je da crevna mikrobiota bude u zdravoj ravnoteži. Ovo je veoma izazovna situacija u kojoj je neophodno biti tolerantan na korisnu floru a sprečiti kolonizaciju patogenih mikroorganizama.
Jedan od najjednostavnijih mehanizama antimikrobne zaštite je prisustvo dvoslojnog sloja sluzi, koji drži luminalne mikrobe udaljenie od kontakta sa epitelom, pretežno u debelom crevu.
Sluz se sastoji od različitih vrsta mucin glikoproteina koje izlučuju peharaste ćelije u crevima i protežu se do 150 µm od epitela debelog creva [9].
Unutrašnji sloj je gušći i ne sadrži nijedan organizam, dok je spoljni sloj dinamičan i sadrži glikone kao izvor hrane za mikro organizme [10].
Suprotno debelom crevu u kome sluz igra važnu ulogu, u tankom crevu veću ulogu imaju antimikrobni proteini, jer je sloj sluzi ovde neprekidan i neadekvatan.
Mikrobiota creva, preko svojih strukturnih komponenti i metabolita indukuju sintezu antimikrobnih proteina (AMP), poput katelicidina, lektina tipa C od strane Panetovih ćelija domaćina.
Mikrobiota creva doprinosi imunomodulaciji zajedno sa urođenim i sa adaptivnim imunim sistemom.
Korisne bakterije u crevima igraju ključnu ulogu u razvoju urođenih imunih ćelija – posebno makrofaga, monocita i neutrofila – specijalnih belih krvnih zrnaca koji pružaju prvu liniju odbrane protiv invazivnih patogena.
Interesantno je videti da ovi mikrobi imaju imuni efekat izvan mesta gde žive u crevima. Utičuju na mesta poput krvi, slezine i koštane srži – mesta gde ne bi trebalo da bude nikakvih bakterija.
Veza između naših bakterija u crevima i imunog sistema je složena i presudna za naše zdravlje.
Nedavne studije su počele da otkrivaju delove ove veze, ali mnogo toga ostaje neotkriveno. Na primer, pronađene su određene dobre bakterije koje regulišu reakciju našeg tela i mozga na stres.
Bakterije creva takođe moduliraju reakciju tela na rak, a studije zumiraju kako podstiču imuni odgovor na malignitete u jetri ili pankreasu.
Kao što neki lekari kažu „ogroman deo vašeg imunološkog sistema je zapravo u vašem gastrointestinalnom traktu“.
Nekoliko faktora doprinosi oblikovanju zdrave mikrobiote creva i to se dinamički odvija tokom celog života pojedinca.
Početni milje od dečije mikrobiote creva posle primarne inokulacije deluje nestabilno i bez raznolikosti, ali sa vremenom se stabilizuje, diverzifikuje i stiče 40% – 60% sličnost sa mikrobiotom odrasle osobe i to do 3. godine života [11].
Naprotiv, pokazala su i istraživanja da bi mala deca i adolescenti mogli da demonstriraju značajne razlike u proporcijama bakteroida i Bifidobacterium u poređenju sa odraslima [12].
Mikrobiota je uglavnom u stabilnom stanju 3. do 7. decenija života, iako proporcija Bifidobacteria, Firmicutes i Fecalibacterium prausnitzii imaju tendenciju smanjenja sa porastom E. coli, Proteobakterije i Stafilokoka [13].
Neke od funkcionalnih uticaja koje vremenom mogu da utiču na promene normalne crevne flore uključuje smanjenu sposobnost da sintetišu vitamin B12, smanjuju aktivnost mikrobne reduktaze, povećana tendencija ka izmeni DNK, povišen stresni odgovor i imunološka disfunkcija [14].
Iako se mikrobiota u početku razvija uglavnom pod uticajem vrste hrane (majčino mleko ili formula) nakon primarne inokulacije, vremenom promene flore zavise od načina ishrane, stila života, životnih događaja (npr stresa) i faktora životne sredine uključujući korišćenje lekova kao što su antibiotici.
Kod novorođenčadi, bakterije koje koloniziraju creva uključuju Bifidobacterium i Lactobacillus i u osnovi, one se razlikuju u zavisnosti od vrste hranjenja.
Kod onih koji su hranjeni mlečnom formulom (adaptirano mleko), Enterokok, Enterobakterije, Bacteroides, Clostridia i drugi anaerobni Streptococcus dominira u crevnoj niši; dok, kod novorođenčadi koja su dojena, Bifidobacterium i Lactobacillus dominiraju.
Stoga usled nenormalne crevne kolonizacije mikrobiote, može doći do pedijatrijskih bolesti usled lošeg imuniteta (15).
Ishrana je i dalje najvažnija odrednica u oblikovanju kompozicije, raznolikosti mikrobiote čak i kod odraslih.
Više od 50% varijacija crevne mikrobiote je vezano za promene u ishrani u odrasloj dobi se na ovaj način može menjati mikrobiota u roku od nekoliko dana. Generalno, unos hrane bogate voćem, povrćem i vlaknima je povezan sa većim bogatstvom i raznolikošću mikrobiote creva.
Pojedinci koji konzumiraju ovu vrstu hrane imaju veće količine mikroorganizama koji metabolišu nesvarljive ugljene hidrate kao što su bakterije iz roda Firmikuta: Ruminococcus bromii, Roseburia i Eubacterium rectale [16].
U jednoj studiji pokazano je da 4-dnevna primena ishrane zasnovane na životinjskim proizvodima je uticala na smanjenje broja firmikuta i porast broja organizma koji tolerišu žučne sokove kao što su Alistipes sp. i Bacteroides sp. iz filuma Bacteroidetes i Bilophila sp. iz filuma Proteobacteria.
Ovo ukazuje da čak i vrlo kratka primena dijetetskog režima može da ima značajan pozitivan uticaj na mikrobiotu creva [17].
Nekoliko studija je pokazalo da postoje značajne geografske i sezonske razlike u mikrobiomima creva. Međutim, ove razlike su bile takođe povezane sa razlikom u načinu ishrane.
Jedno od glavnih svojstava zdrave crevne mikrobiote je sposobnost da konkurentno isključuje patogene. [18].
Još pre četiri decenije je pokazano da bi antibiotici mogli da poremete normalnu floru i time da prekinu konkurencije za isključenje patogena, što je dovelo do infekcije npr.salmonelom odmah nakon antibiotske terapije.
Jedan od mogućih razloga za ovakav događaj može biti gubitak široke mreže interakcije među bakterijskim vrstama, koje su podstakle proizvodnju sialne kiseline pogodne za rast patogena poput Salmonella typhimurium i Clostridium difficile [19].
Velike promene mikrobiote creva kao odgovor na antibiotike uključuje smanjene taksonomske raznolikosti i dugotrajne promene u znatnom delu crevne flore pojedinaca.
Dokazano je da čak i kratkotrajna antibiotska terapija (od 7 dana) širokog spectra anaerobnog delovanja (npr. Clindamicin) može da utiče na promenu mikrobiote creva i do 2 godine sa nepovratnim diverzitetom Bacteriodes-a [20].
Slično tome, terapija za Helicobacrter pylori koja uključuje najčešće trostruku terapiju antibioticima jedan od njih je klaritromicin, pokazalo je da dramatično smanjuje raznolikost Aktinobakterije sa povećanjem rezistentnog gena erm B od hiljadu puta [21].
Efekat ciprofloksacina koji ima pretežno gram-pozitivna pokrivenost naglo smanjuje broj ruminokoka u crevima [22].
Svetska zdravstvena organizacija definiše probiotike kao žive mikroorganizme koji mogu da pruže korist ljudskom zdravlju ako se daju na adekvatan način i u pravim količinama.
Nekoliko vrsta poput Lactobacillus casei, Lactobacillus planatarum, Lactobacillus bulgaricus, Lactobacillus acidophilus, Bifidobacterium longum, Bifidobacterium infantis, Streptococcus thermophilus, E. coli sojNissle 1917, su pokazali da imaju imunomodulatornu efekat kao efekat na crevnu barijeru.
Probiotici se koriste komercijalno kao dodatak za kontrolisanje ili tretiranje određenih zdravstvenih stanja npr. iritabilan kolon (IBS), inflamatorna bolest creva (IBD), proliv povezan sa antibioticima itd.
Pobiotici sprečavaju dejstvo patogenih bakterija tako što ometaju vezivanje ovih bakterija za sluznicu creva, menjaju pH creva i podstiču lučenje bakteriocina, supstance koja direktno uništava patogene bakterije u crevima.
Takođe probiotici smanjuju stvaranje citokina koje dovode do zapaljenja, a stimulišu sintezu antitela u crevima i to sekretornog IgA. Dodavanje prebiotika bi eventualno moglo pojačavaju efekat probiotika.
Prebiotici su nesvarljive materije (fermentisani oligosaharidi) koji su posebno dizajnirani da promene sastav i aktivnost crevne flore sa namerom da se promoviše zdravlje domaćina.
Bakterije creva selektivno fermentiraju ova vlakna proizvodeći kratkolančane masne kiseline (SCFA), koja zauzvrat daje pozitivan efekat na zdravlje creva.
Kada dođe do narušavanja crevne mikrobiote usled različitih faktora (bilo da je to hronično bolesno stanje, česta upotreba antibiotika, stila života, načina ishrane), najvažnije je pristupiti problemu individualno.
Pre primene određene terapije idealno bi bilo uraditi analizu gastrointestinalne funkcije i sastava crevnog mikrobioma.
Detaljna analiza stolice (CDSA) je napredni test koji nudi sveobuhvatan pregled celokupnog zdravlja gastrointestinalnog (GI) traktata. Ovaj profil stolice pruža informativan i fleksibilan pregled gastrointestinalnih funkcija.
Analizom se ocenjuje:
CDSA ™ analiza je procena odabranog skupa biomarkera stolice. Ova analiza stolice procenjuje: Markere za varenje / apsorpciju, metaboličke markere creva mikrobiološke markere creva.
CDSA može otkriti važne kliničke informacije o uzrocima mnogim uobičajenim simptomima kao što su: gasovi, nadimanje, bol u stomaku, diareje i opstipacije.
Analiza “ Detaljna analiza stolice (CDSA)“ vam je dostupna u svim Beo-lab laboratorijama. Oviu analizu pomežete da poručite i online preko e-laboratorije.
Test ne zahteva nikakvu posebnu pripremu. Analiza se vrši na bazi jednog uzorka stolice.
Uzorak je potrebno dostaviti u posebnu posudicu za fekalni uzorak (dobićete specijalni komplet za uzorkovanje).
Na rezultate analiza se čeka do 21 dana. Više o ovom testu pročitajte u opisu analize u okviru e-laboratorije.
Tradicionalno GI testiranje zahteva napredne postupke za obradu slika i neprijatne postupke ispitivanja koji mogu biti skupi.
Mikrobiota i detaljna analiza stolice CDSA nudi jednostavan način da se kliničarima pruži vredan uvid u neravnoteže gastrointestinalnog trakta.
CDSA test stolice pruža trenutne, primenljive kliničke informacije za pacijente koji se žale na gastrointestinalne probleme. Pomaže kliničarima u utvrđivanju uzroka probavnih tegoba i podržava identifikaciju ciljanih tretmana.
GI Effects® sveobuhvatni profil stolice je napredni test stolice koji pruža trenutne, delotvorne kliničke informacije za upravljanje gastrointestinalnim zdravljem.
Koristeći vrhunske tehnologije i biomarkere, ovaj test nudi dragocen uvid u probavne funkcije, crevne upale i crevni mikrobiom.

Sveobuhvatni profil stolice GI Effects može pružiti važne informacije o osnovnom uzroku mnogih uobičajenih gastrointestinalnih simptoma kao što su gasov, nadimanje, probavne smetnje, bol u stomaku, diareje i opstipacije.
Ova analiza stolice koristi biomarkere kao što je kalprotektin da bi se razlikovala inflamatorna bolest creva (IBD) i sindrom iritabilnog creva (IBS) ili disbioza.
Intestinalni mikrobi su zavisni jedan od drugog kao i od ljudskog domaćina, a zdravlje jednih utiče na drugo. Znatan obim istraživanja povezuje disbiozu ili neuravnotežen i mikrobiom creva s višestrukim stanjem bolesti unutar i izvan GI trakta.
Različite metaboličke aktivnosti mikrobioma na kraju utiču na ljudsko zdravlje i ljudsko zdravlje na kraju utičue na zdravlje mikrobiote.
GI Effect ( mikrobiota) analiza stolice detaljno testira bakterije, gljivice, parazite GI trakta koristeći PCR, kultivaciju i mikroskopske metode.
Određuju se marker i mikroorganizmi koji precizno daju informaciju o gastrointestinalnoj funkciji:
GI Effect (mikrobiota) analiza stolice vam je dostupna u svim Beo-lab laboratorijama . Navedenu analizu možete zakazati i putem e-laboratorije.
Test ne zahteva nikakvu posebnu pripremu. Analiza se radi na 3 uzastopna uzorka stolice.
Za uzorak stolice dobićete specijalni komplet za uzorkovanje sa uputstvom za korišćenje.
Na rezultate analiza se čeka do 21 dana.
SAZNAJ VIŠE
Preporučujemo vam da pročitate i o testu : Disbioza kao uzrok digestivnih smetnji.
Reference:
Ukoliko Vam se sviđa članak podelite ga sa prijateljima.
4,550.00din
7,600.00din
3,350.00din
2,100.00din
6,150.00din
Samo u Beo-lab laboratorijama laboratorijske analize možete poručiti onlajn.
